Reemplazo total de cadera primario con superficies metal-metal de segunda generación
REVISTA ACARO | VOL 3, Nº 4: 189-192 | 2017
Reemplazo total de cadera primario con superficies metal-metal de segunda generación
Roberto Olivetto, Javier M. Olivetto, Adrián L. Olivetto
Javier Olivetto
javierolivetto@hotmail.com
RESUMEN
Introducción: Los pares de fricción metal-metal de segunda generación fueron introducidos en 1988 por B.G. Weber, con el propósito de reducir el desgaste y evitar la osteólisis inducida por partículas de polietileno en reemplazos totales de cadera.
Materiales y Métodos: Se operaron 110 pacientes a los que se les realizaron 118 reemplazos totales de cadera primarios no cementados con superficie articular metal-metal, entre septiembre del 1995 a diciembre de 2011. La edad media de dichos pacientes al tiempo de la cirugía fue de 52 años. De estos pacientes 69 cumplieron con los criterios de inclusión, la implantación de una prótesis CLS tallo Spotorno con cotilo expansivo, cabeza de 28 mm (Metasul ; Zimmer) y 10 o más años de seguimiento.
Resultados: Tres cotilos (4.34 %) debieron ser revisados, 2 por aflojamiento aséptico del implante combinado con ostelólisis local y el restante por defectos técnicos en la colocación. La media del Harris Hip Score obtenido fue de 90.6 puntos a los 10 años, con un valor pre-operatorio medio de 51.2 puntos. La tasa de supervivencia de los implantes fue del 95.66 % a los 15 años post operatorio.
Conclusión: Los resultados clínicos y radiográficos obtenidos en nuestro estudio en reemplazos totales de cadera con uso de superficies metal-metal son comparables con los publicados en la literatura para otras superficies duras.
Nivel de Evidencia: IV
Palabras clave: Artroplastia de Cadera; Metal-Metal; No Cementado
INTRODUCCIÓN
Las superficies articulares Metal-Metal de segunda generación fueron introducidas en 1988 por B. G. Weber, con la finalidad de reducir el desgaste del par articular y evitar la osteólisis inducida por partículas de polietileno en los reemplazos totales de cadera.1
Las aleaciones de Cromo – Cobalto – Molibdeno generan una mejor lubricación articular en comparación con las superficies articulares metálicas de primera generación. En pruebas de simulación articular en laboratorio, los pares de fricción metal-metal (Metasul; Zimmer) produjeron 100 veces menos partículas de desgaste volumétrico que el par metal-polietileno.2
Los pacientes con superficies articulares metal–metal poseen niveles superiores de cromo y cobalto, tanto en sangre como en orina, en comparación con pacientes con pares de fricción metal – polietileno o grupos control no operados3,4 Esto genera la potencial aparición de hipersensibilidad adquirida, mutaciones genéticas, carcinogénesis y la aparición de pseudotumores.5-8 Sin embargo, numerosas publicaciones han descripto que dichos efectos adversos son escasos con el uso de superficies metal–metal de segunda generación.9-12
El objetivo de este trabajo fue proporcionar información sobre la supervivencia a largo plazo, los resultados clínicos y el aspecto radiográfico en nuestro grupo de pacientes con un seguimiento mínimo de 10 años.
MATERIALES Y MÉTODOS
Pacientes
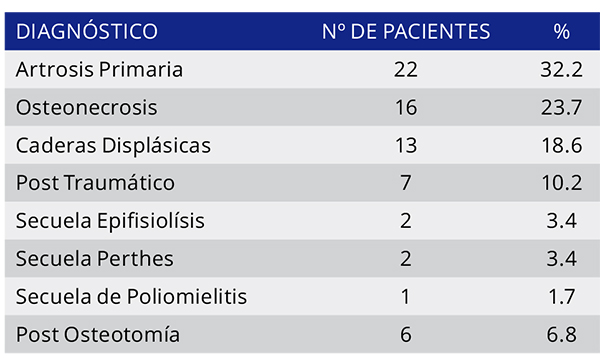
Entre septiembre del 1995 a diciembre de 2011 se realizaron 118 artroplastias de cadera (110 pacientes) no cementadas utilizando prótesis con alta concentración de carburos y una superficie articular Metal-Metal. De dichos pacientes 69 cumplieron con los criterios de inclusión que fueron, el uso de prótesis metal–metal de segunda generación (Metasul; Zimmer) con cabeza de 28 mm y un seguimiento mínimo de 10 años. De los pacientes incluidos la media para la edad fue de 52 años, se operaron 36 hombres y 33 mujeres. El diagnóstico más común fue la artrosis primaria (32.2%), seguida por la osteonecrosis (23.7%) y la displasia de cadera en tercer lugar (18.6%) (Tabla 1).
Todas las cirugías fueron realizadas por vía posterolateral, con los pacientes en decúbito lateral, por el mismo equipo quirúrgico y en la misma institución.
TABLA 1: DIAGNÓSTICOS
Implante
Se utilizó el tallo femoral Modelo Spotorno , un cotilo CLS expansivo que contiene una copa metálica recubierta de polietileno de ultra alto peso molecular y una cabeza metálica de 28 mm Cr Co Mo (Metasul; Zimmer).
La estabilidad primaria de los componentes femorales y acetabulares está dada por fijación a presión (press-fit) luego de una adecuada preparación en el área de implantación ósea.
Evaluación Clínica y Radiográfica
La información clínica fue obtenida a través de las Historias Clínicas y los controles periódicos de los pacientes en consultorio con un seguimiento mínimo de 10 años y un 90 máximo de 21 años. Todos los pacientes fueron evaluados mediante el Harris Hip Score pre y postoperatorio.13
Se tomaron radiografías anuales de cadera (anteroposteriores y laterales) en busca de cambios en la estructura ósea así como cambios en el posicionamiento de los componentes. Se utilizaron las zonas de Gruen para el fémur y la clasificación de DeLee-Charnley para el componente acetabular.14,15 También se evaluó la aparición de calcificaciones heterotópicas según la clasificación de Brooker.16
Análisis de Sangre
No se obtuvieron muestras de sangre para medir los niveles de Cromo y Cobalto en ninguno de los casos. Solo se consideró para aquellos pacientes con sintomatología de aflojamiento y radiografías positivas para ello. Los valores obtenidos fueron inferiores a 7 µg/L. En dichos casos también se realizaron ecografías de cadera para descartar la aparición de posibles pseudotumores.17
Análisis Estadístico
Para el análisis estadístico de los resultados se utilizó el método de Kaplan–Meier, teniendo en cuenta la revisión de cualquiera de los dos componentes protésicos así como el tiempo de seguimiento de los pacientes.18
RESULTADOS
De los 69 pacientes estudiados se perdió el seguimiento de 3 de ellos, quedando un total de 66 pacientes evaluados. Se realizaron 3 revisiones a nivel del componente acetabular y ninguna que comprometa el tallo femoral. Dos de estas revisiones fueron debido a un aflojamiento mecánico con valores de laboratorio y cultivos normales para infección, a los 8 y 10 años post operatorios. El caso restante fue debido a la falla técnica en la colocación de implante acetabular en una paciente obesa y se realizó a los 2 años post operatorios.
La media de Harris Hip Score de los pacientes fue de 95.6 puntos para la totalidad de los mismos y se obtuvo un score de 90.6 para aquellos que superaron los 10 años de seguimiento.73
Se obtuvieron 57 radiografías para su evaluación con un seguimiento mínimo de 10 años. Se encontraron imágenes radiolúcidas predominantemente en las zonas 1 (16%), 7 (5%) y 8 (7%) (fig. 1), e imágenes osteolíticas en las zonas 1 (3%), 6, 7 (1.7%) y 8 (1.3%) (fig. 2). A nivel acetabular se observaron imágenes radiolúcidas a nivel de las zonas II (1%) y III (7%) de DeLee-Charnley (fig. 3). Se identificaron áreas de osteólisis a nivel de las zonas I y II en el 2% y 3% de los casos respectivamente. La inclinación media del componente acetabular fue de 47 grados. En un sólo paciente se observaron calcificaciones heterotópicas grado 2 de Brooker.
La probabilidad de sobrevida de estos implantes a los 10 años post operatorios fue de 98.3%.

Figura 1
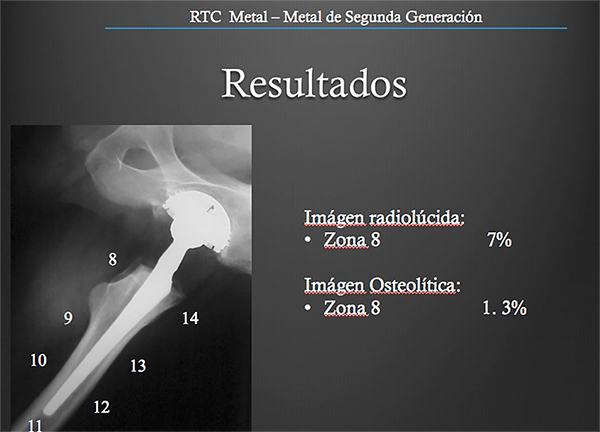
Figura 2
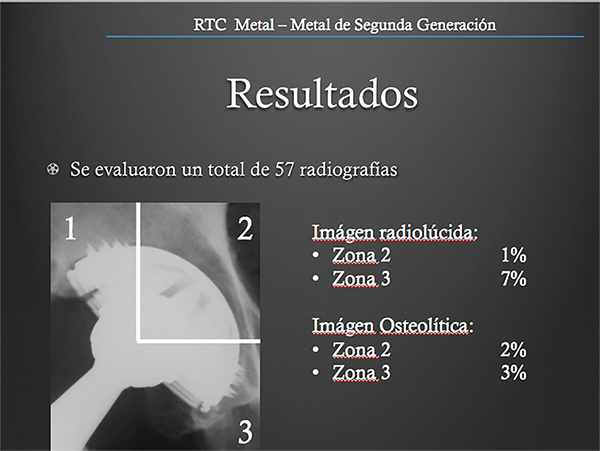
Figura 3
DISCUSIÓN
A pesar de la disminución en el índice de desgaste generado por este tipo de par articular, el aflojamiento mecánico es la causa más frecuente de revisión a predominio del componente acetabular.19 Numerosas publicaciones respaldan el uso de superficies metal sobre metal con cabezas protésicas entre 28 y 32 mm de diámetro, ya que con las mismas se han reportado pocas reacciones adversas, bajos niveles iónicos en sangre y se han obtenido resultados clínicos excelentes con seguimientos de 25 años.11,12,20
En la bibliografía no se halló relación en cuanto a la actividad de los pacientes y los niveles iónicos en sangre.21-23 Hart y col.24 publicaron que el ángulo de inclinación del componente acetabular se encontraría en relación directa con los niveles metálicos en sangre.
Con respecto al análisis radiográfico realizado en nuestro estudio, encontramos líneas radiolúcidas predominantemente en la región proximal de los tallos (zonas 1, 7 y 8 de Gruen). No se encontraron cambios en la radiolucencia, ni lesiones osteolíticas en las zonas distales. Se encontró correlación en dos componentes acetabulares con imagen de aflojamiento y clínica positiva que debieron ser revisados, manteniendo el par Metal-Metal en uno de los casos y pasando a una articulación Cerámica – Polietileno en el otro.
Numerosos autores han reportado que los niveles iónicos tienden a disminuir con el tiempo, hallando valores de cobalto con un seguimiento de 5 años de 0.89 µg/L en comparación con valores de 0.58 µg/L en el mismo estudio con seguimiento a largo plazo.9,25
Como limitación de nuestro estudio encontramos la falta de la evaluación de los niveles séricos metálicos en nuestra población de pacientes y la variabilidad en el tiempo de seguimiento de nuestro grupo, con pacientes con un seguimiento mínimo de 10 años y máximo de 21 años.
Como fortalezas se puede enumerar que la cohorte etaria fue homogénea, que fue operada y evaluada por el mismo equipo quirúrgico y el mismo modelo de implante protésico y que se controlaron los pacientes a mediano y largo plazo.
CONCLUSIONES
Los resultados clínicos y radiográficos obtenidos en nuestro estudio en reemplazos totales de cadera con uso de superficies metal-metal son comparables con los publicados en la literatura para otras superficies duras.
Numerosas publicaciones han informado sobre la seguridad del uso de articulaciones Metal sobre Metal de segunda generación con tiempos de seguimiento mayores a 25 años. La aparición de nuevos implantes metálicos, la modularidad a nivel de los cuellos y el incremento de cabezas protésicas metálicas de gran tamaño trajo consigo la aparición de nuevas y más frecuentes complicaciones que han logrado demonizar el uso de la superficie Metal – Metal.
Creemos que el uso de dichas superficies deberían ser tenido en cuenta para ciertas indicaciones particulares, con las recomendaciones ya estudiadas por numerosos autores, utilizando implantes que han demostrado bajo riesgo de complicaciones a lo largo del tiempo.
BIBLIOGRAFÍA
- Schmidt M, Weber H, Schon R. Cobalt chromium molybdenum metal combination for modular hip prostheses. Clin. Orthop. Relat. Res. 1996:S35-47.
- Anissian HL, Stark A, Gustafson A, Good V, Clarke IC. Metal-on-metal bearing in hip prosthesis generates 100-fold less wear debris than metal-on-polyethylene. Acta Orthop. Scand. 1999;70:578-582.
- Brodner W, Bitzan P, Meisinger V, Kaider A, Gottsauner-Wolf F, Kotz R. Elevated serum cobalt with metal-on-metal articulating surfaces. J. Bone Joint Surg. Br. 1997;79:316-
- Brodner W, Bitzan P, Meisinger V, Kaider A, Gottsauner-Wolf F, Kotz R. Serum cobalt levels after metal-on-metal total hip arthroplasty. J. Bone Joint Surg. Am. 201 2003;85-a:2168-2173.
- Visuri T, Pukkala E, Paavolainen P, Pulkkinen P, Riska EB. Cancer risk after metal on metal and polyethylene on metal total hip arthroplasty. Clin. Orthop. Relat. Res. 1996:S280-289.
- Signorello LB, Ye W, Fryzek JP, et al. A nationwide followup study of autoimmune and connective tissue disease among hip and knee implant patients. J. Long. Term Eff. Med. Implants. 2002;12:255-262.
- Davies AP, Sood A, Lewis AC, Newson R, Learmonth ID, Case CP. Metal-specific differences in levels of DNA damage caused by synovial fluid recovered at revision arthroplasty. J. Bone Joint Surg. Br. 2005;87:1439-1444.
- Willert HG, Buchhorn GH, Fayyazi A, et al. Metal-on-metal bearings and hypersensitivity in patients with artificial hip joints. A clinical and histomorphological study. J. Bone Joint Surg. Am. 2005;87:28-36.
- Lass R, Grubl A, Kolb A, et al. Primary cementless total hip arthroplasty with second-generation metal-on-metal bearings: a concise follow-up, at a mínimum of seventeen years, of a previous report. J. Bone Joint Surg. Am. 2014;96:e37.
- Grubl A, Marker M, Brodner W, et al. Long-term follow-up of metal-on-metal total hip replacement. J. Orthop. Res. 2007;25:841-848.
- Paleochorlidis IS, Badras LS, Skretas EF, Georgaklis VA, Karachalios TS, Malizos KN. Clinical outcome study and radiological findings of Zweymuller metal on metal total hip arthroplasty. a follow-up of 6 to 15 years. Hip Int. 2009;19:301-308.
- Girard J, Bocquet D, Autissier G, Fouilleron N, Fron D, Migaud H. Metal-on-metal hip arthroplasty in patients thirty years of age or younger. J. Bone Joint Surg. Am. 2010;92:2419-2426.
- Harris WH. Traumatic arthritis of the hip after dislocation and acetabular fractures: treatment by mold arthroplasty. An end-result study using a new method of result evaluation. J. Bone Joint Surg. Am. 1969;51:737-755.
- Gruen TA, McNeice GM, Amstutz HC. “Modes of failure” of cemented stem-type femoral components: a radiographic analysis of loosening. Clin. Orthop. Relat. Res. 1979:17-27.
- DeLee JG, Charnley J. Radiological demarcation of cemented sockets in total hip replacement. Clin. Orthop. Relat. Res. 1976:20-32.
- Brooker AF, Bowerman JW, Robinson RA, Riley LH, Jr. Ectopic ossification following total hip replacement. Incidence and a method of classification. J. Bone Joint Surg. Am. 1973;55:1629-1632.
- Muraoka K, Naito M, Nakamura Y, Hagio T, Takano K. Usefulness of ultrasonography for detection of pseudotumors after metal-on-metal total hip arthroplasty. J. Arthroplasty. 2015;30:879-884.
- Kaplan EL, Meier P. Nonparametric Estimation from Incomplete Observations. Journal of the American Statistical Association. 1958;53:457-481.
- Malviya A, Ramaskandhan J, Holland JP, Lingard EA. Metal-on-metal total hip arthroplasty. J. Bone Joint Surg. Am. 2010;92:1675-1683.
- Delaunay CP. Metal-on-metal bearings in cementless primary total hip arthroplasty. J. Arthroplasty. 2004;19:35-40.
- Heisel C, Silva M, Skipor AK, Jacobs JJ, Schmalzried TP. The relationship between activity and ions in patients with metal-on-metal bearing hip prostheses. J. Bone Joint Surg. Am. 2005;87:781-787.
- Vendittoli PA, Mottard S, Roy AG, Dupont C, Lavigne M. Chromium and cobalt ion release following the Durom high carbon content, forged metal-on-metal surface replacement of the hip. J. Bone Joint Surg. Br. 2007;89:441-448.
- Imanishi T, Hasegawa M, Sudo A. Serum metal ion levels after second-generation metal-on-metal total hip arthroplasty. Arch. Orthop. Trauma Surg. 2010;130:1447-1450.
- Hart AJ, Ilo K, Underwood R, et al. The relationship between the angle of version and rate of wear of retrieved metal-on-metal resurfacings: a prospective, CT-based study. J. Bone Joint Surg. Br. 2011;93:315-320.
- Savarino L, Padovani G, Ferretti M, et al. Serum ion levels after ceramic-on-ceramic and metal-on-metal total hip arthroplasty: 8-year minimum follow-up. J. Orthop. Res. 2008;26:1569-1576.